【CMT&CHTV 文献精粹】
导语:视网膜疾病,如年龄相关性黄斑变性、糖尿病视网膜病变、青光眼和葡萄膜炎,长期以来被认为与适应性免疫系统中的T细胞驱动过程密切相关。然而,最新的研究证据显示,天然免疫反应在这些疾病的发生发展中起着至关重要的作用。炎症小体作为一种能够响应细胞应激的敏感细胞内警报系统,由不同的蛋白组成,在遇到病原体入侵或内源性应激信号时迅速组装成多蛋白复合体,发出强烈的激活信号,引发焦亡。焦亡是一种程序性细胞死亡过程,与凋亡不同,其特征是细胞肿胀、膜破裂和细胞内容物的释放。在视网膜疾病中,炎症小体和焦亡的激活与炎症的发生密切相关。
2024年4月,Progress in Retinal and Eye Research发表了"Targeting inflammasomes and pyroptosis in retinal diseases—molecular mechanisms and future perspectives"一文,深入探讨了视网膜疾病中炎症小体和焦亡(pyroptosis)的分子机制及其作为未来治疗视角的潜力。

研究设计
本综述采用了系统性文献回顾的方法,对现有的科学文献、临床试验和实验室研究结果进行了深入分析。研究者用关键词如“inflammasomes”、“pyroptosis”、“retinal diseases”等,检索了包括但不限于PubMed、Web of Science和Scopus等,搜集了过去几十年间的文献资料。
研究采用了定性和定量分析相结合的方式,同时关注不同研究间的异质性,并对可能的偏倚风险进行了评估。在患者特征方面,研究者回顾了不同研究中涉及的患者群体,包括年龄、性别、疾病类型和病程等信息。此外,还关注了不同研究中采用的干预措施,如药物治疗、基因治疗或其他新型治疗手段,以及这些干预措施对炎症小体和焦亡的影响。
研究结果
炎症小体在视网膜疾病中的激活
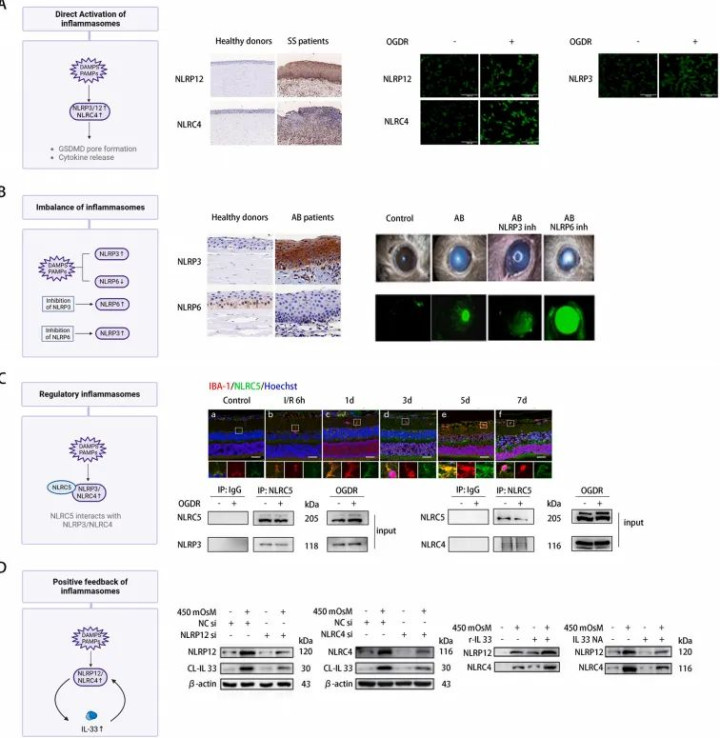
研究揭示了炎症小体在多种视网膜疾病中的激活情况。例如,在青光眼患者中,NLRP3炎症小体的表达水平显著升高,与视网膜神经节细胞(RGCs)的死亡密切相关。糖尿病视网膜病变(DR)患者中,NLRP3炎症小体的激活与血管内皮细胞的损伤和血管渗漏有关。此外,在年龄相关性黄斑变性(AMD)患者中,NLRP3炎症小体的激活与视网膜色素上皮细胞(RPE)的功能障碍相关。
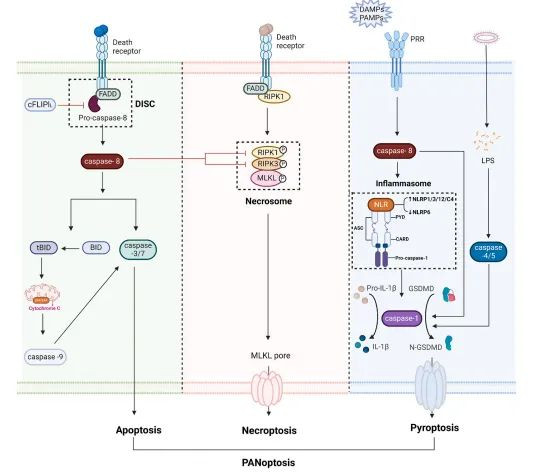
焦亡途径的关键分子
研究识别了焦亡途径中的关键分子,包括caspase-1、GSDMD和炎症因子IL-1β和IL-18。在糖尿病视网膜病变模型中,高血糖诱导的NLRP3/caspase-1/GSDMD途径导致血管周细胞死亡。在AMD模型中,炎症小体激活导致IL-1β和IL-18的成熟和释放,进而促进病变发展。
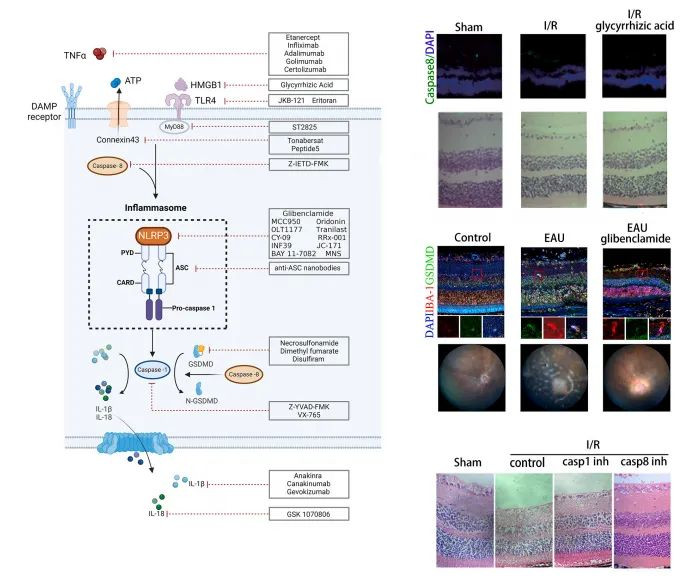
抗炎治疗的潜在靶点
研究结果指出了抗炎治疗的潜在靶点,如Kaempferol能够通过促进NLRP3的自噬降解来抑制炎症小体的激活,减少视网膜缺血/再灌注(I/R)损伤。此外,Connexin43模拟肽通过减少血管内皮细胞死亡和血管渗漏来增强视网膜神经节细胞的存活。
炎症小体与焦亡的相互作用
研究进一步探讨了炎症小体与焦亡之间的相互作用。例如,caspase-8在决定细胞命运中起着关键作用,不仅促进凋亡途径的激活,还抑制坏死途径,并且在焦亡中通过激活炎症小体和直接切割GSDMD家族蛋白来发挥作用。
治疗策略的临床前研究在临床前研究中,药物如MCC950通过特异性抑制NLRP3炎症小体,显示出对眼部组织的保护作用。Epac1和PKA激动剂如forskolin通过降低NEK7水平来减少NLRP3炎症小体的活性。此外,TNFAIP3通过降低TLR4和NEK7的表达来抑制NLRP3炎症小体的激活。
总结讨论
研究强调了炎症小体和焦亡在视网膜疾病中的重要作用,并指出了针对这些途径的治疗策略的潜力。尽管目前的治疗手段,如抗VEGF疗法和免疫抑制剂在一定程度上能够控制炎症,但针对炎症小体和焦亡的特定抑制剂可能会提供更有效的治疗选择。未来的研究需要进一步探索这些途径在不同视网膜疾病中的具体作用机制,并开发出更加精准的靶向治疗策略。
参考文献:Sun Y, Li F, Liu Y, et al. Targeting inflammasomes and pyroptosis in retinal diseases-molecular mechanisms and future perspectives[J]. Prog Retin Eye Res. 2024;101:101263. doi:10.1016/j.preteyeres.2024.101263

